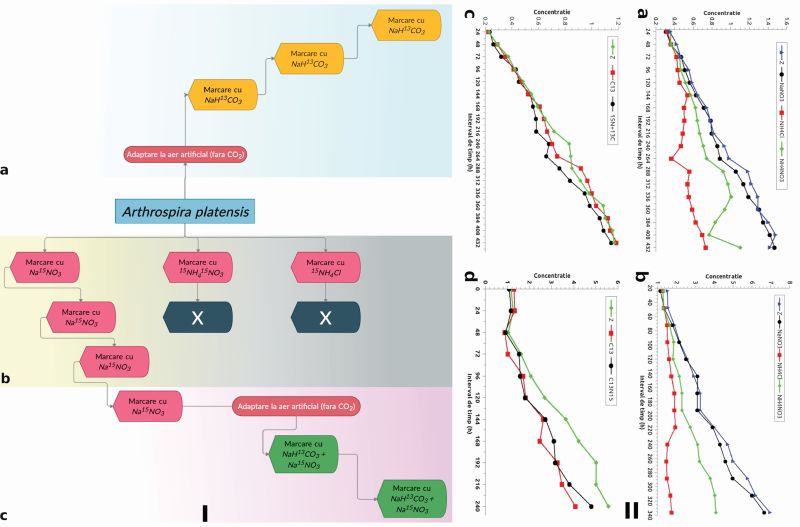
Faza 1: Separarea avansată a izotopului 13C pe o cascadă de trei coloane utilizând fracțiuni de diferite concentrații izotopice și conversia produsului la 13CO2 pentru aplicații bio-chimice.
Valoare fază: 1.745.914 lei
Termen de încheiere: 12.09.2019
Rezultate:
(i) realizarea schemei și a configurației de alimentare și conectare a coloanelor în serie;
(ii) stabilirea parametrilor de operare;
(iii) punerea în operare a instalației, alimentarea continuă, extragerea produsului și evacuarea deșeului;
(iv) bază de date experimentale pentru funcționare instalației cu coloane în paralel;
(iv) realizarea unei instalaţii experimentale pentru oxidarea CO la CO2;
(v) testarea catalizatorilor în reacţia de oxidare a CO nemarcat la CO2;
(vi) caracterizarea catalizatorilor utilizați.
(ii) Diseminare: 1 comunicare științifică prezentată la o conferință internațională și 1 acceptată:
• A. Balla, C. Marcu, J. Zs. Szucs-Balazs, C. Varodi, C. Lar, Ş. Bugeac, M. Miheţ, D.M. Lazăr, G. Borodi, Carbon monoxide oxidation over Ni/Al2O3 catalyst: determination of activation energy, RomCat 2019, 5-7 Iunie, 2019, Bucureşti, România;
• Ș. Bugeac, J. Zs. Szücs-Balázs, C. M. Varodi, C. Lar, M. C. Marcu, A. C. Balla, M. L. Gligan, Commissioning of a cryogenic distillation cascade for separation of carbon stable isotopes, PIM 2019, 25-27 Septembrie, 2019, Cluj-Napoca, România.